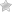Аутоиммунный тиреоидит у детей младше 13 лет встречается достаточно часто, его практически невозможно диагностировать на ранних стадиях в связи с отсутствием специфических симптомов. Клетки щитовидной железы постепенно разрушаются, из-за чего она перестает производить гормоны. При своевременном начале лечения заболевания прогноз благоприятный.
При лечении аутоиммунного тиреоидита у детей поможет употребление витаминов.
Причины
Хронический аутоиммунный тиреоидит не может возникнуть из-за неправильного образа жизни самого пациента. В основе патологического процесса лежит нарушение функций иммунитета, при котором он начинает вырабатывать антитела, уничтожающие здоровые клетки щитовидной железы. Способствуют запуску воспалительного процесса следующие факторы:
- Наличие наследственной предрасположенности. Считается главной причиной развития аутоиммунного тиреоидита. Риск возникновения этой патологии многократно повышается, если она имеется у родителей ребенка.
- Психоэмоциональные перегрузки.
- Возраст и половая принадлежность пациента. Аутоиммунный тиреоидит часто диагностируется у девочек старше 7 лет.
- Бактериальные и вирусные инфекции. Длительное течение инфекции негативно отражается на состоянии иммунитета, из-за чего он начинает работать некорректно.
- Проживание в неблагоприятной экологической обстановке. Иммунная система не всегда способна справиться с нейтрализацией токсичных веществ.
Симптомы
При нормальной выработке гормонов каких-либо признаков тиреоидита не появляется. Единственным неудобством становится изменение контуров шеи, создающее дискомфорт при ношении одежды с воротником и шарфов. В остальных случаях заболевание имеет следующие симптомы:
- Бледность кожных покровов лица. На щеках и носу ребенка появляется нездоровый румянец.
- Заторможенность реакций. Движения пациента неуклюжие, замедленные, отсутствует интерес к подвижным играм.
- Ухудшение состояния волос. Они становятся редкими и ломкими, начинают выпадать. В редких случаях наблюдается поредение бровей.
- Нарушение мимики. Во время разговора лицо ребенка практически не меняет выражения.
При аутоиммунном тиреоидите у детей во время разговора лицо ребенка практически не меняет выражения.
- Нарушение речи, связанное с отеком языка. Орган увеличивается в размерах и утолщается, на боковых его частях появляются следы от зубов. Речь пациента становится невнятной.
- Снижение интеллектуальных способностей. Родители начинают замечать, что дети плохо учатся, долго вспоминают названия предметов и явлений.
- Отек слизистых оболочек носа, препятствующих нормальному дыханию.
- Одышка, брадикардия.
- Бледность и сухость кожи тела. Эластичность тканей снижается, образуются грубые складки. Возможно появление сухих пятен и трещин в области крупных суставов.
- Повышенная утомляемость, постоянная усталость, снижение работоспособности, сонливость.
- Нарушение пищеварения. Недостаток тиреоидных гормонов способствует замедлению перистальтики кишечника, из-за чего часто возникают запоры. Помочь в таком случае могут только слабительные и клизмы.
- Позднее половое созревание у подростков.
Позднее половое созревание у подростков может быть симптомом аутоиммунного тиреоидита у детей.
Диагностика аутоиммунного тиреоидита у детей
Для выявления аутоиммунного тиреоидита используются следующие диагностические методики:
- Первичный осмотр и сбор анамнеза. Позволяет обнаружить признаки разрастания тканей ЩЖ, изменения во внешнем виде пациента.
- Общий анализ крови. Отражает характерные для аутоиммунного воспаления изменения — снижение уровня лейкоцитов, повышение количества лимфоцитов.
- Анализ крови на гормоны. На ранних стадиях наблюдается увеличение концентрации тиреоидных гормонов. При дальнейшем развитии тиреоидита активность щитовидки снижается, из-за чего уровень Т3 и Т4 падает.
- Иммунограмма. Используется для обнаружения сбоев в работе иммунной системы.
- УЗИ. В ходе процедуры обнаруживается изменение размеров щитовидки, неравномерность ее структуры.
- Тонкоигольная биопсия. В исследуемом образце присутствует повышенное число лимфоцитов и других клеток, свидетельствующих о течении аутоиммунной агрессии.
- Гистологическое исследование. Необходимо для своевременного выявления злокачественного перерождения воспаленных тканей.
УЗИ способно обнаруживать изменение размеров щитовидной железы, неравномерность ее структуры.
Лечение
Устранить аутоиммунную патологию полностью невозможно, поэтому лечение имеет симптоматический характер. Эндокринолог назначает следующие препараты:
- Средства заместительной гормональной терапии. L-тироксин восполняет недостаток тироксина и трийодтиронина, необходимых для нормального функционирования всего организма.
- Препараты йода.
- Тиростатики (Мерказолил, Тиамазол). Применяются в период обострения, сопровождающегося повышением активности железы.
Таблетки мерказолил применяются в период обострения, сопровождающегося повышением активности железы.
- Противовоспалительные средства (Индометацин, Диклофенак). Уменьшают интенсивность аутоиммунного воспаления путем подавления выработки антител.
- Иммуномодуляторы, витамины.
Хирургическое вмешательство назначается при выраженном увеличении щитовидной железы, из-за которого ребенок испытывает сложности при глотании.
Народные средства
При аутоиммунном тиреоидите применяются следующие народные средства:
- Морская капуста. Ее перетирают в порошок и добавляют во все блюда.
- Настойка грецких орехов. 200 г измельченного сырья заливают 0,5 л водки, настаивают 3 недели в темном прохладном месте. Принимают по 5-10 капель, предварительно растворяя препарат в 1 ст. воды.
- Свежевыжатые фруктовые и овощные соки. Благотворно влияют на общее состояние организма. Преимуществом подобных лекарственных средств является приятный вкус, что важно при лечении детей раннего возраста.
Диета при аутоиммунном тиреоидите
Рацион должен обеспечивать потребность организма в питательных веществах и иметь высокую калорийность. Не стоит отказываться от мясных и рыбных блюд, кисломолочных продуктов. В меню при аутоиммунном тиреоидите включают большое количество овощей и фруктов, содержащих витамины и микроэлементы. Главным продуктом питания становятся каши, сваренные на воде или молоке.
Источник: https://schitovidka03.ru/bolezni/tireoidit/vidy/autoimmunniy/deti
Аутоиммунный тиреоидит у детей: причины, характерные симптомы и методы лечения эндокринной патологии
Любой признак гормональных нарушений в детском возрасте – повод обратиться к врачу
В современном мире наблюдается тенденция к «омоложению» многих болезней: так, проблемы с щитовидкой встречаются у школьников и даже новорожденных малышей. Среди всей эндокринной патологии значительное место занимает аутоиммунный тиреоидит у детей: лечение заболевания требует внимательного отношения со стороны врача, так как вызывает стойкую дисфункцию органа.
В нашем подробном обзоре и видео в этой статье рассмотрим причины, механизм развития, симптомы, а также современные принципы диагностики и терапии этого гормонального расстройства.
Подробнее об АИТ
Аутоиммунный тиреоидит (иначе АИТ) – хроническое заболевание, характеризующееся выработкой аутоантител к тиреоглобулину и тиреопероксидазе и медленным необратимым угнетением функций щитовидной железы.
Это интересно. Впервые заболевание было описано в 1942 году японским врачом Хакара Хашимото. Позднее хроническое аутоимунное поражение щитовидки было названо в его честь.
АИТ у детей встречается приблизительно в 0,2-4% случаев. Чаще болезнь развивается у девочек-подростков, но может встречаться и у детей дошкольного возраста. 70-80% случаев первичного приобретенного гипотиреоза у детей являются следствием аутоиммунного поражения щитовидной железы.
Часто щитовидка начинает «барахлить» в подростковом возрасте, когда происходит мощный гормональный всплеск
В настоящее время патогенез развития заболевания изучен не до конца. Доказано, что главную роль в формировании аутоиммунного тиреоидита играет генетическая предрасположенность.
Факторами, которые запускают процесс ауотоагрессии к собственным клеткам щитовидной железы, являются:
- стрессы;
- изнуряющие физические нагрузки;
- вирусные и бактериальные инфекции;
- гормональные перестройки;
- неблагоприятная экологическая обстановка.
Воздействие причинного фактора запускает цепочку патологических реакций:
- Выработка антител собственной защитной системой организма.
- Атака клетками иммунитета тиреоглобулина и тиреоидной пероксидазы – ключевых веществ, отвечающих за выработку гормонов щитовидки.
- Развитие хронического воспаления тканей щитовидки в ответ на повреждение.
- Компенсаторное разрастание здоровых тканей эндокринного органа для обеспечения потребностей организма в тиреоидных гормонах.
- Хроническое необратимое угнетение всех функций щитовидной железы, замещение клеток органа соединительной тканью.
Классификация
Существует несколько классификаций заболевания, все они используются в медицинской практике.
Таблица: Классификация аутоиммунного тиреоидита:
| Тип классификации | Виды тиреоидита | Описание |
| По функциональной активности ЩЖ | Эутиреоидный | Функция щитовидной железы не нарушена |
| Гипертиреоидный | Наблюдается повышенная активность ЩЖ – гипертиреоз. Непродолжительная стадия, вызванная массивным разрушением тиреоидных клеток и выделением в кровь большого количества гормонов | |
| Гипотиреоидный | Угнетение всех функций ЩЖ. При АИТ носит хронический, прогрессирующий характер | |
| По степени увеличения ЩЖ | Гипертрофическая | Характеризуется разрастанием тканей ЩЖ, формированием зоба |
| Атрофическая | Сопровождается атрофией – отмиранием тканей ЩЖ и значительным уменьшением размеров органа | |
| По течению | Латентный | Протекает скрыто, не имеет клинических проявлений |
| Клинический | Протекает с яркой симптоматикой |
Клинические проявления
Тиреоидит щитовидной железы у детей развивается постепенно. Первые несколько лет заболевание никак себя не проявляет. Типичное течение патологии включает несколько синдромов.
Зоб
Зоб – равномерное увеличение размеров щитовидки – обычно первое, чем проявляет себя аутоиммунный тиреоидит: симптомы у детей могут включать:
- дискомфорт, болезненные ощущения в шее;
- дисфагию – нарушение глотания;
- одышку, затруднение дыхания;
- заметное увеличение размеров шеи, которое можно определить своими руками и даже на глаз.
На ощупь железа обычно имеет ровную поверхность, но может быть и бугристой, узловатой.
Зоб у ребенка (на фото) развивается постепенно
Обратите внимание! Рост щитовидной железы при аутоиммунном тиреоидите происходит постепенно, поэтому часто ни маленькие пациенты, ни их родители не замечают патологических изменений.
Гормональные расстройства
При патологии встречаются самые разнообразные гормональные расстройства. Для ранней стадии заболевания, сопровождающейся массивным разрушением клеток щитовидки, типичен тиреотоксикоз у детей: симптомы его могут быть следующими:
- беспричинное беспокойство, повышенная тревожность;
- плаксивость, капризность;
- нарушения сна, кошмары;
- повышение аппетита, сопровождающееся снижением массы тела;
- тахикардия – увеличение ЧСС;
- подрагивание кончиков пальцев, языка;
- повышенная потливость.
Обратите внимание! В отличие от гипертиреоза при диффузном токсическом зобе, увеличение концентрации тиреоидных гормонов в крови не сопровождается глазной симптоматикой – экзофтальмом и неполным смыканием век.
В дальнейшем уровень гормонов в крови падает, и деструктивных гипертиреоз сменяется недостатком функции щитовидной железы:
- замедлением обмена веществ, набором лишнего веса;
- сонливостью, подавленностью;
- ухудшением памяти и внимания, снижением успеваемости;
- брадикардией, гипотонией.
Если успеваемость вашего школьника резко ухудшилась, возможно, дело в больной щитовидке
Согласно статистике, у детей с АИТ функция щитовидной железы снижается на 3-5%.
Это интересно. Аутоиммунный тиреоидит у дошкольников и подростков имеет более благоприятное течение, чем у взрослых. Примерно у четверти больных с клиническим гипотиреозом происходит спонтанное восстановление всех эндокринных функций щитовидки.
Диагностика
Врачебная инструкция предписывает проводить следующие виды обследования всем детям с подозрением на аутоиммунный гипотиреоз:
- Общие клинические анализы крови и мочи.
- Б/х анализ крови с определением мочевины, креатинина, АЛТ, АСТ, общего билирубина, панкреатической амилазы.
- Анализ крови на тиреоидные гормоны — Т3, Т4, ТТТ (см. Как сдать анализы на гормоны щитовидной железы правильно).
- Анализ крови на антитела к тиреоглобулину и тиреопероксидазе – основной лабораторный метод диагностики АИТ.
- УЗИ щитовидной железы.
Средняя цена комплексного обследования щитовидки в частной клинике –3000 р.
Согласно рекомендациям Американской Ассоциации эндокринологов, значимыми критериями для постановки диагноза АИТ являются:
- Увеличение размеров щитовидной выше возрастных норм.
- Превышение титра анти-ТПО стандартных значений (0-30 ед/мл) более, чем в 2 раза.
- Наличие УЗ-критериев АИТ:
- снижение эхогенности;
- участки гипер- и изоэхогенности;
- присутствие фиброзных тяжей.
Лечение
Терапия аутоиммунного поражения щитовидной железы у детей основывается на следующих принципах:
- Следование здоровому образу жизни: полноценное питание, прогулки на свежем воздухе, физическая активность, закаливание.
- Полноценное витаминизированное питание.
- Своевременная санация хронических очагов инфекции;
- При тиреотоксикозе – назначение тиреостатиков (стандартная доза Мерказолила для подростка – 0,5 мг/кг/сут.). Курс лечения – 2-3 недели.
- При гипотиреозе – длительная заместительная терапия препаратами левотироксина в дозировке 3-5 мг/кг/сут.
Обратите внимание! Хотя активные разработки в этом направлении ведутся уже несколько десятилетий, эффективное лекарство, которое вмешивается в защитную систему организма и подавляет защитные процессы, пока не создано.
Проблемой номер один в эндокринологии остается аутоиммунный тиреоидит: лечение у детей этой патологии занимает одно из приоритетных направлений в медицинской практике. Ранняя диагностика и следование рекомендациям врача в вопросах терапии заболевания позволяют добиться стойкой компенсации состояния ребенка и восстановления нормального гормонального фона.
Источник: https://Schitovidka.su/zabolevaniya/deti/autoimmunnyj-tireoidit-u-detej-36
Аутоиммунный тиреоидит у детей, подростков, симптомы и питание при аутоиммунном тиреоидите
Тиреоидит у подростков развивается не реже, чем у взрослых, но, объясняя симптомы болезни начавшимся половым созреванием, к врачу обращаются с опозданием. Патология представляет опасность отягощением состояния другими нарушениями эндокринной и сердечно-сосудистой системы. При подозрении на дисфункцию щитовидной железы следует посетить эндокринолога. На ранней стадии развития АИТ хорошо реагирует на проводимое лечение.
Причины развития
У девочек аутоиммунный тиреоидит возникает вдвое чаще, чем у мальчиков. Мониторинг позволил выявить, что развитию патологии более подвержены дети старше 6 лет.
Причины появления аутоиммунного тиреоидита у подростков – наследственная предрасположенность, стрессовый фактор.
Другие провоцирующие обстоятельства:
- неблагоприятная экологическая обстановка;
- у девочек – становление менструального цикла;
- недосыпание;
- изнурительный труд;
- механическое повреждение щитовидной железы;
- перенесенная интоксикация (пищевая, лекарственная);
- воспаление органов ЖКТ;
- низкокачественное питание.
Немаловажное значение имеет наличие сопутствующих патологий. Особенно тех, которые относятся к эндокринной системе. Риск развития АИТа у подростков повышается, если одновременно прогрессирует дисфункция коры надпочечников, гипофиза, поджелудочной железы.
В развитии болезни определяющее значение имеет состояние защитных свойств организма.
Симптомы
Заболевание протекает постепенно, его симптомы длительное время могут оставаться незамеченными.
Клинические проявления аутоиммунного тиреоидита у подростков:
- Выраженный дискомфорт в горле, ощущение наличия в нём комка, который препятствует глотанию, дыханию и разговору.
- Проблемы с запоминанием, концентрацией внимания.
- Прощупываемое уплотнение в горле.
- Сухость слизистых оболочек полости рта (но ощущение жажды – отсутствует).
- Замедленная речь, обильное выпадение волос, ломкость ногтей, разрушение зубов. Перечисленные признаки вызваны недостаточностью кальция в крови, что развивается на фоне АИТа.
- Повышенная сухость и бледность кожи (иногда ткани принимают восковой оттенок).
- Частый кашель, имеющий приступообразный характер (начинается с лёгкого першения в горле).
- Появление отёков на лице, запястьях и голеностопных суставах.
- Изменение пищеварения (периодически возникают эпизоды запора или наоборот – диареи).
- Нарушение сна, перемены настроения.
- Учащение сердцебиения, повышение показателей артериального давления.
- Обильное выделение пота (преимущественно ночью).
В редких случаях наблюдается повышение температуры тела, тошнота, рвота, снижение веса.
Перечисленные признаки чётко указывают на дисфункцию щитовидной железы. На основании озвученных жалоб пациента и данных осмотра, врач уже может поставить предварительный диагноз. Но для подтверждения заключения специалиста, пациента направляют на обследование.
Диагностика
При подозрении на наличие ювенильного тиреоидита, подростку предстоит пройти лабораторное, аппаратное, инструментальное исследование:
- УЗИ щитовидной железы. Быстро и точно устанавливает её размер, строение, однородность тканей.
- Анализ крови на определение гормонов ЩЖ (Т3, Т4 и ТТГ). Устанавливает повышение или наоборот – снижение концентрации этих веществ.
- Исследование крови на определение антитиреоидных гормонов.
- Анализ мочи на установление концентрации йода.
- МРТ щитовидной железы. Назначают при наличии сомнений относительно критериев органа (кровоснабжения, структуры).
Дополнительно выполняют мониторинг показателей артериального давления, пульса и дыхания.
Чтобы исключить наличие злокачественного опухолевого процесса, проводят тонкоигольную биопсию с последующим гистологическим исследованием.
Предварительно выполняют обезболивание – для снижения степени неприятных ощущений. Затем тонкой иглой берут небольшую часть уплотнения щитовидной железы и направляют на исследование. Анализ позволяет в точности определить, каково происхождение новообразования – злокачественное или доброкачественное.
Лечение
Госпитализация при аутоиммуном тиреоидите показана только при выявлении злокачественной опухоли щитовидной железы и при нарастающей асфиксии. Лечение делится на консервативный вид и хирургическое вмешательство.
Консервативная терапия и операция
Гормонотерапию и симптоматическое лечение проводят только при подтверждении наличия доброкачественного процесса. Благоприятный прогноз обеспечивает введение L-тироксина и применение препаратов противовоспалительного действия. Нестероидные средства сокращают выработку антитиреоидных антител, что способствует выздоровлению.
Особенности питания
Меню диетического питания, с учётом ежедневного объёма йода, составляет врач-эндокринолог.
При дефиците микроэлемента в организме, в меню следует включить ламинарию, морскую рыбу, запечённый картофель, морковь, мясо индейки.
Профилактика аутоиммунного тиреоидита у подростков
Риск развития АИТа можно сократить, если:
- Улучшить качество питания подростка.
- Регулярно организовывать отдых в благоприятных экологических зонах.
- Не допускать переутомления.
- Избегать интоксикации всех видов. Не перегружать организм ребёнка лекарствами.
Важно своевременно купировать воспалительные заболевания абсолютно всех желез внутренней секреции.
При своевременном устранении патологии удастся избежать двух основных осложнений АИТа – лимфомы щитовидной железы и гипотиреоза.
Источник: https://gormons.ru/zhelezy/shhitovidnaya-zheleza/autoimmunnyj-tireoidit-u-detej-podrostkov-simptomy/
Хронический аутоиммунный тиреоидит у детей | #07/99 | Журнал «Лечащий врач»
Хронический аутоиммунный тиреоидит (ХАТ) в прежние годы считался уделом взрослых и, как правило, не диагностировался в детском возрасте. В настоящее время резко выросла частота ХАТ у детей и подростков.
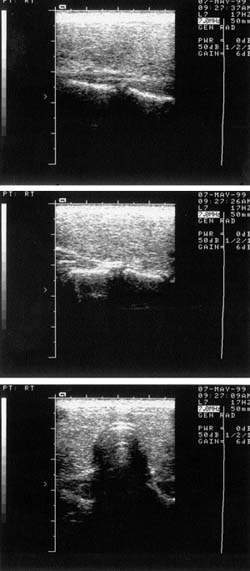
| Рисунок 1. Увеличение щитовидной железы III степени |
Впервые аутоиммунное поражение щитовидной железы (ЩЖ) было описано Хашимото в 1972 году у четырех женщин. Автор назвал это заболевание «struma lymphomatosa». В нашей стране струму Хашимото впервые описал в 1954 году С. Б. Пинский у девочки 13 лет.
При накоплении клинических данных по аутоиммунному поражению ЩЖ появился ряд различных классификаций, из которых наиболее удачной считается классификация R. Volpe (1984).
В ее рубрикации ХАТ подразделяется на несколько различных форм, среди которых специально выделяется лимфоцитарный тиреоидит детей и подростков.
Известно, что ХАТ по системе HLA ассоциируется с локусами B8, DR5, DR3, так же как и многие другие аутоиммунные заболевания, причем ассоциация с локусом DR5 обусловливает гипертрофическую, а с локусом DR3 — атрофическую форму ХАТ.
Наследственный генез болезни подтверждается данными о частных случаях заболевания у близких родственников (Л. А. Лисенкова). В родословной больных ХАТ нередко регистрируются и другие аутоиммунные заболевания эндокринного и соматического генеза.
Генетически обусловленный дефект иммунокомпетентных клеток ведет к срыву естественной толерантности. Этот процесс может быть запущен перенесенной вирусной инфекцией, реже травмой ЩЖ или операцией на ЩЖ.
Однако убедительных данных об этиологии ХАТ до настоящего времени не существует.
При этом заболевании происходит выработка антител (АТ) к тиреоглобулину, к тиреоидной пероксидазе ЩЖ, известны АТ ко II коллоидному антигену (АГ), к гормонам ЩЖ — Т3, Т4, к рецепторам тиреотропного гормона (ТТГ) на мембранах тиреоцитов.
Однако наибольшее значение в цитотоксическом эффекте придается АТ к тиреоидной пероксидазе (ТПО) ЩЖ, что в сочетании с другими нарушениями иммунобиологических реакций приводит в конечном итоге к деструкции клеток ЩЖ и снижению ее функции — к гипотиреозу.
Это состояние приводит к повышенному выбросу ТТГ гипофизом, который провоцирует рост сохранившегося тиреотропного эпителия с последующей инфильтрацией его лимфоцитами, макрофагами, плазматическими клетками.
При гистологическом исследовании ЩЖ при ХАТ обнаруживается диффузная или очаговая инфильтрация лимфоцитами и плазматическими клетками с нахождением типичных для этого процесса гипертрофированных оксифильных эпителиоидных клеток Ашкенази — Гюртля. В зависимости от фазы и длительности процесса можно обнаружить фиброз стромы ЩЖ.
Заболевание имеет постепенное хроническое течение и гораздо чаще встречается у лиц женского пола. У детей ХАТ может нередко развиваться в дошкольном и младшем школьном возрасте, но с преобладанием частоты возникновения в пре- и пубертатном периоде.
Постепенное развитие болезни в начальном периоде может сопровождаться признаками нарушения функции ЩЖ. Считается, что меньшая выраженность гипотиреоза у детей и в дальнейшие периоды развития болезни обусловлена более высокой способностью клеток фолликулярного эпителия к регенерации.
Клиническая диагностика ХАТ у детей основана на синдроме увеличения ЩЖ (рис. 1). В настоящее время рекомендуется пользоваться классификацией размеров зоба по данным пальпации, предложенным ВОЗ (1994).
Согласно критериям ВОЗ, выделяются следующие определения размеров ЩЖ: степень 0 — зоба нет, степень I — размеры долей ЩЖ больше дистальной фаланги большого пальца обследуемого пациента, но не видны на глаз, степень II — зоб пальпируется и виден на глаз.
При ХАТ у детей размеры зоба чаще соответствуют II степени увеличения долей ЩЖ.
Несмотря на то что хроническое течение болезни в конечном счете приводит к гипотиреозу, в определенных фазах заболевание может проявляться и как гипертиреоз. Особенностью течения ХАТ у детей и подростков является более частая регистрация фазы тиреотоксикоза.
Это явление получило название хаштоксикоза в отличие от аналогичных проявлений при диффузном токсическом зобе. В этих случаях на фоне увеличения ЩЖ отмечается тахикардия, изменение АД с увеличением пульсового давления, потливость, тремор век и пальцев вытянутых рук и др.
Как правило, в этой фазе ХАТ не регистрируется экзофтальм — один из типичных симптомов диффузного токсического зоба (ДТЗ).
Известно также, что тиреотоксическая фаза ХАТ имеет значительно более короткие сроки, чем при ДТЗ, и обусловлена поступлением в кровь, при деструкции клеток ЩЖ, большого количества ранее синтезированного гормона.
В последующем может наступить спонтанная ремиссия, а затем постепенное развитие гипотиреоза через фазу его субклинического течения. Признаками гипотиреоза являются: появление брадикардии, снижение АД, тенденция к запорам, зябкость, холодные конечности, меньшая подвижность ребенка — синдром брадипсихизма, снижение успеваемости в школе.
| Рисунок 2. Ультразвуковая картина хронического аутоиммунного тиреоидита |
Пальпация увеличенной ЩЖ может определять различный характер ее консистенции в зависимости от фазы и длительности болезни. Типичным считается наличие плотной консистенции ЩЖ, ее неоднородность, узловатость, иногда легкая болезненность.
При тиреотоксической фазе болезни железа может быть менее плотной или плотно-эластической консистенции.
Диагноз подтверждается исследованием ультразвуковой (УЗИ) картины ЩЖ, которая выявляет увеличение органа; неоднородность эхоструктуры с наличием гипоэхогенных участков, иногда сочетающихся с гиперэхогенными; нечеткость контуров ЩЖ; наличие узлов в ткани ЩЖ у детей встречается значительно реже (рис. 2).
Для определения функции ЩЖ необходимо исследование в сыворотке крови концентрации гормонов ЩЖ — тироксина (Т4), трийодтиронина (Т3), а также ТТГ и тироксинсвязывающего глобулина (ТСГ).
При гипертиреоидной фазе болезни можно обнаружить повышение уровней Т4 и Т3 и, как правило, значительное снижение ТТГ и ТСГ. При гипофункции диагностическим тестом является повышение ТТГ иногда при нормальном уровне Т4 и Т3 (субклический гипотиреоз) или при одновременном снижении уровня тиреоидных гормонов.
Доказательством аутоиммуного генеза болезни служит исследование уровня АТ к тиреоглобулину, но большее значение имеет повышенный уровень АТ к тиреоидной переоксидазе.
Если при пальпации и тем более УЗИ возникает подозрение на узлы, рекомендуется проведение тонкоигольной безаспирационной биопсии подозрительных участков ЩЖ с последующим морфологическим исследованием.
В специализированной эндокринологической клинике Морозовской детской клинической больницы и детском отделении эндокринологического диспансера Москвы проведен клинико-лабораторный и инструментальный анализ особенностей течения ХАТ у 154 детей в возрасте от 8 до 15 лет за период с 1991 по 1998 год. Изучение родословной этого контингента детей выявило семейную отягощенность по патологии ЩЖ у родственников 65% больных.
У абсолютного большинства детей увеличение ЩЖ соответствовало II степени по классификации ВОЗ. Пальпация ЩЖ показала наличие плотно-эластической консистенции ЩЖ у 75% детей, у 14% детей — подозрение на узлы. У 11% детей отмечалась болезненность при пальпации.
Состояние функции ЩЖ при поступлении в клинику в первые годы наблюдения у 31% расценивалась как тиреотоксическая фаза, частота обнаружения которой в последние три года наблюдения увеличилась до 60%.
Клиника Хаш-токсикоза чаще имела среднетяжелую степень выраженности и лишь у единичных детей — тяжелую. У 20% выявлена субклиническая или легкая клиническая фаза гипотиреоза, у остальных 20% обследованных нарушений функций ЩЖ не обнаружено.
Однако отмечалась тенденция к более высоким нормальным показателям ТТГ, что также могло расцениваться как субклинический гипотиреоз.
УЗИ у всех обследованных подтвердило типичную для ХАТ картину. Интерес представляло увеличение объема ЩЖ у больных детей по сравнению с возрастными нормативами в зависимости от фазы заболевания.
При эутиреозе увеличение объема ЩЖ было в два-четыре раза больше нормальных величин; при гипотиреозе — в три-пять раз больше, при легком тиреотоксикозе — в полтора-два раза, при среднетяжелой степени тиреотоксикоза было обнаружено наиболее значительное увеличение объема ЩЖ, превышающее у детей в 10-12 раз нормальные возрастные показатели.
Аутоиммунный характер болезни не всегда подтверждался нахождением высоких титров АТ к тиреоидной пероксидазе или тиреоглобулину.
Исследование трех классов иммуноглобулинов (M, G, A) не имело информативного значения. Пункционная безаспирационная биопсия, проведенная у детей, у которых пальпаторно или при УЗИ имелись подозрения на узлы или было значительное увеличение ЩЖ, выявила типичную лимфоидную инфильтрацию, в том числе и при исследовании узловой ткани.
Явлений фиброза не было отмечено ни в одном из наблюдений, что подтверждает лимфоцитарный характер аутоиммунного тиреоидита у детей и подростков, специально выделенный по классификации ХАТ и, возможно, обуславливающий благоприятный прогноз в отдаленном будущем при адекватном лечении болезни.
Лечение в условиях стационара проводилось соответственно фазе течения ХАТ.
В фазу гипертиреоза использовали коротким курсом в две-три недели мерказолил, в последние годы применяли метизол в средних лечебных дозах — не более 0,5 мг на 1 кг массы тела в сутки в три приема под контролем клинического наблюдения и гормонального тиреогенеза.
При достижении эутиреоидного состояния тиреостатики отменялись, и назначались малые дозы L-тироксина (25, в дальнейшем 75 мкг в сутки). При тиреотоксикозе использовались также b-адреноблокаторы, обладающие способностью снижать периферическую трансформацию Т4 в Т3 и тем положительно влиять на лечение.
Учитывая аутоиммунный генезис болезни, можно рекомендовать использование нестероидных противовоспалительных препаратов, а также антибактериальных при наличии болезненности ЩЖ или очагов хронической инфекции, что практически наблюдается у всех детей с ХАТ.
В фазе субклинического и явного гипотиреоза основным лечением был прием L-тироксина в дозе от 100 до 150 мкг в сутки под контролем уровня ТТГ, Т4, Т3. Адекватность назначенного лечения в основном контролировалась уровнем ТТГ через один-два месяца от начала терапии.
Лечение тиреоидными препаратами рекомендуется проводить длительно, учитывая хронический характер течения заболевания.
Глюкокортикоидные препараты, как правило, не имеют применения и используются в комплексе лечения при выраженной болезненности ЩЖ, сочетании ХАТ с отечным экзофтальмом (что крайне редко встречается у детей) или при неэффективности адекватной длительной терапии.
Проведена специальная работа Н. А. Сакаевой (1989), показавшая положительное значение применения иммунокорректоров (Т-активин) как в комплексе с тиреоидными препаратами, так и в виде монотерапии в фазе эутиреоза ХАТ.
Хирургическое лечение считается не показанным при ХАТ. У 75% детей, по данным Ф. Г. Садыкова, развивается тяжелый гипотиреоз. Исключением может быть только быстрорастущий зоб, сдавление увеличенной ЩЖ трахеи или сосудов шеи, а также подозрение на рак при наличии узлов. Дети, больные ХАТ, должны находиться под постоянным диспансерным наблюдением педиатра-эндокринолога.
Литература 1. Жуковский М. А. Детская эндокринология. М.: Медицина, 1982. С. 103-105. 2. Садыков Ф. Г. Заболевание щитовидной железы у детей и подростков. Автореф. дис. … докт. мед. наук. М., 1989. 3. Сакаева Н. А. Состояние иммунологического статуса при аутоиммунном и подостром тиреоидитах и возможность его коррекции применением иммуномодулятора Т-активина: Автореф. дис. … канд. мед. наук. М., 1989. 4. Руководство по клинической эндокринологии / Под ред. проф. Н. Т. Старковой. Спб.; М.; Харьков; Минск, 1996. С. 164-169. 5. Volpe R. The thyreoid and autoimmunity. Amsterdam, 1986.
Источник: https://www.lvrach.ru/1999/07/4527973/
Аутоиммунный (ювенильный) тиреоидит у подростков
Хронический ювенильный тиреоидит (аутоиммунный, лимфоцитарный) — самая распространенная патология эндокринной системы среди детей и подростков, в основе которой лежит гиперплазия щитовидной железы (юношеский зоб).
Аутоиммунный тиреоидит чаще всего у подростков развивается на фоне приобретенного гипотиреоза.
Причины ювенильного тиреоидита
Помимо вышеназванного приобретенного гипотиреоза, причинами заболевания могу являться специфические не часто встречающиеся в этом возрасте патологии, такие как
- фелиноз,
- туберкулез,
- эпидемический паротит,
- саркоидоз.
Также патогенез ювенильного тиреоидита может быть обусловлен гормональными изменениями в организме подростков, что характерно для полового созревания.
Острое течение тиреоидита встречается крайне редко. Обычно такому течению заболевания предшествует инфекционная патология дыхательных органов.
- В большинстве случаев поражение охватывает левую часть железы, в редких случаях в ней формируется гнойный абсцесс.
- Для острого течения тиреоидита свойственна головная боль и физическое ограничение двигательных способностей головы и шеи, отечность, покраснение и выраженная болезненность в области щитовидной железы.
- В крови развивается стойкий лейкоцитоз.
- Если провести сцинтиграфию эндокринного органа, то можно обнаружить, что поврежденные ткани железы не в полном объеме поглощают нуклиды, а УЗИ-диагностика свидетельствует о наличии сложной эхогенной структуры.
- Функциональные возможности железы не изменяются, но гнойная форма тиреоидита может привести к тиреотоксикозу у подростка, обусловленного увеличением продуцируемых гормонов разрушенными тиреоидитом тканями.
- Иногда этиология ювенильного тиреоидита так и остается не выясненной, у детей развиваются клинические признаки гипотиреоза, нередко сопровождающиеся отставанием в росте.
Симптомы аутоиммунного тиреоидита
Хронический тиреоидит чаще встречается среди девочек — до 7 раз чаще, чем у мальчиков. Впервые болезнь может проявить себя уже в трехлетнем возрасте, но чаще всего болеют дети, достигшие 6 лет и старше.
- В подростковом возрасте отмечается максимум заболевания, специфическими признаками которого является гиперплазия и отставание в росте.
- Зоб растет в медленном темпе, его размеры могут варьироваться.
- Щитовидная железа на практике диффузно увеличена, отличается повышенной плотностью и безболезненностью.
- У многих детей диагностируется эутиреоз, но клинические симптомы выражены слабо или отсутствуют.
В некоторых случаях отмечаются жалобы на компрессионный синдром шеи. Лабораторная диагностика показывает картину гипотиреоза.
Симптомы гипотиреоидного состояния наблюдаются у трети пациентов:
- раздражительность и нервозность,
- гиперактивный синдром,
- потливость и пр.
Крайне редко ювенильному тиреоидиту сопутствует базедова болезнь, однако офтальмопатия встречается у подростков и без этого заболевания.
Клиническая картина заболевания может варьироваться. Зоб может сохранять свой размер, может уменьшаться с возрастом, однако больные остаются годами в состоянии эутиреоза или гипотиреоза.
- В 25% всех случаев заболеваний, ювенильный тиреоидит имеет наследственную семейную природу.
- Скорее всего, выработка аутоантител к тканям щитовидной железы и йодидпероксидазе передается по наследственной линии от мужчин.
- В таких семьях нередко одновременно присутствуют больные ювенильным и лимфоцитарным тиреоидитом, а также диффузным токсическим зобом и гипотиреозом, — этот факт в очередной раз доказывает то, что все эти эндокринные заболевания имеют под собой единую основу.
Тиреоидит у детей и подростков нередко сочетается с такими патологиями, как алопеция, витилиго и пернициозная анемия.
Лечение
- При диагностированном гипотиреозе назначается заместительная терапия препаратами йода, натриевой солью и синтезированными гормонами железы.
- На фоне лечения зоб, скорее всего, будет регрессировать, но возможно он останется и неизменным на протяжении многих лет.
- Лечение тиреотоксикоза также проводится специфическими препаратами, направленными на снижение гиперсекреции эндокринного органа.
- Также возможно развитие стойкой ремиссии, так как антитиреоидные антитела могут менять свой количественный состав в крови в зависимости от эффективности лечения.
- Пациенты, которые не нуждаются в специфической терапии, должны динамически обследоваться.
- Узловые изменения железы, возникшие ранее и сохраняющиеся при проведении лечения, необходимо исследовать с помощью тонкоигольной биопсии, чтобы исключить риск развития злокачественного процесса.
Источник: https://proshhitovidku.ru/zabolevaniya/yuvenilnyj-tireoidit
Аутоиммунный тиреоидит у детей
Актуальность проблемы
Заболевания щитовидной железы (ЩЖ) занимают лидирующее положение среди всей эндокринной патологии у детей, а первое место в их структуре принадлежит диффузному нетоксическому зобу (ДНЗ).
В большинстве регионов России ДНЗ регистрируется более чем у 5% детей препубертатного возраста, что обусловлено наличием в этих территориях зобной эндемии, связанной как с дефицитом йода в окружающей среде, так и с экологическим неблагополучием [1,2,3].
ДНЗ является гетерогенным состоянием, включающим наряду с эндемическим зобом аутоиммунный тиреоидит (АИТ) и дисгормональный зоб.
https://www.youtube.com/watch?v=lUJMlErAQiU
Важнейшим событием в отечественной тиреоидологии в 1999 г.
явилось принятие консенсуса “Эндемический зоб у детей: терминология, диагностика, профилактика и лечение” [4], четко определившего диагностическую и терапевтическую тактику педиатра общей практики при этой патологии. В то же время АИТ у детей до сих пор представляет собой серьезную проблему как в диагностическом, так и в лечебном плане.
Частота клинически явных форм АИТ в популяции составляет около 1%, число больных женщин превышает количество мужчин в 4-8 раз [5, 6, 7]. Распространенность АИТ у детей в различных странах равна 0,1-1,2%. В экологически неблагополучных регионах России отмечается рост заболеваемости АИТ, частота которого в детской популяции достигает 3-5% [8,9].
Сведения о частоте АИТ как у взрослых, так и у детей весьма противоречивы и зависят, в первую очередь, от диагностических возможностей конкретной клиники. По данным диспансерного учета в Москве за 1991-1995 г.г. АИТ выявлялся у 7% детей с тиреоидной патологией [10].
Среди детей и подростков европейской части России, имеющих ДНЗ, диагноз АИТ был установлен в 10-34% случаев [2, 8].
Этиология и патогенез
АИТ является одним из классических аутоиммунных заболеваний. Согласно теории R.Volpe заболевание развивается у наследственно предрасположенных лиц вследствие клеточных и гуморальных иммунологических нарушений. Генетическая обусловленность АИТ подтверждается ассоциацией его с антигенами системы HLA, чаще DR3 и DR5.
Повышенная частота АИТ у женщин возможно отражает связь между генами Х-хромосомы и развитием аутоиммунного процесса, а также влияние эстрогенов на функцию В-лимфоцитов [5, 7].
Под воздействием неблагоприятных факторов генетически обусловленные дефекты иммунокомпетентных клеток ведут к срыву естественной толерантности и инфильтрации щитовидной железы макрофагами, лимфоцитами, плазматическими клетками, образованию антител к тиреоглобулину, микросомальным белковым структурам фолликулярного эпителия.
Циркулирующие аутоантитела кооперируются на поверхности клеток фолликулярного эпителия с Т-лимфоцитами-киллерами и оказывают цитотоксическое воздействие на гормональноактивные клетки щитовидной железы, вызывают деструктивные изменения в тиреоцитах. Следствием этих процессов является снижение функции щитовидной железы.
Уменьшение выработки тиреоидных гормонов стимулирует повышение синтеза ТТГ с последующим развитием зоба [5, 11]. Так формируется гипертрофический вариант АИТ, впервые описанный Хашимото и получивший его имя. У детей в подавляющем большинстве случаев выявляется гипертрофическая форма АИТ. Выделяют также атрофическую форму АИТ и послеродовый тиреоидит.
Типичным морфологическим признаком АИТ является диффузная или очаговая инфильтрация щитовидной железы лимфоцитами и плазматическими клетками, характерно также наличие больших оксифильных клеток Ашкенази.
Согласно данным морфологического исследования ткани щитовидной железы М.Э.
Бронштейн выделяет 3 основных гистологических варианта АИТ: классический (в 2 формах: диффузный и диффузно-узловой), хронический лимфоматозный тиреоидит и хронический лимфоматозный струмит [12].
Особенности клинического течения АИТ у детей
Течение АИТ в детском и подростковом возрасте имеет ряд особенностей. Заболевание характеризуется постепенным началом, медленным прогрессированием, увеличение щитовидной железы может быть умеренным и выявляться у ребенка случайно.
Жалоб дети, как правило, не предъявляют. При наличии жалоб они носят, в основном, неспецифический характер и обусловлены сопутствующей патологией, чаще всего симптомами вегето-сосудистой дистонии.
Симптомы сдавления окружающих органов и тканей при АИТ у детей встречаются нечасто – при больших размерах зоба.
В большинстве случаев АИТ у детей железа при пальпации мало отличается от ДНЗ, поверхность ее гладкая, контуры четкие. Классические пальпаторные признаки АИТ (неровная, бугристая поверхность железы, неоднородность консистенции) в детском возрасте встречаются нечасто [8, 11]. Поэтому решающее значение в диагностике АИТ у детей принадлежит дополнительным лабораторно-инструментальным методам.
У подавляющего большинства детей и подростков с начальной стадией АИТ клинические признаки нарушения функции щитовидной железы отсутствуют и сохраняется эутиреоидное состояние. Однако в каждом пятом случае диагностируется субклинический гипотиреоз [2].
При этом у пациента нет явных клинических симптомов гипофункции щитовидной железы, и гипотиреоз диагностируется на основании повышения уровня ТТГ в сыворотке крови, тогда как уровень тиреоидных гормонов (Т3, Т4) может оставаться в пределах нормы.
У небольшого числа пациентов ранние стадии АИТ могут протекать с гипертиреозом.
Дети с АИТ в фазе субклинического и явного гипотиреоза, так же как больные другими формами ДНЗ, часто отстают в физическом, половом и интеллектуальном развитии, а также в 1,5-2 раза чаще сверстников имеют различные хронические соматические заболевания [3, 8, 9].
Девочки пубертатного возраста, больные АИТ, в 30% случаев имеют различные нарушения полового созревания: либо отставание в половом развитии и запаздывание менархе, либо нарушения овариально-менструального цикла по типу гипоменструального синдрома, вторичной аменореи [13].
- При узловых формах зоба у детей также весьма вероятно их сочетание с АИТ [14], что требует проведения определенных дополнительных методов обследования.
- Основные методы диагностики АИТ у детей
- Диагностика АИТ у детей должна основываться на комплексном обследовании, направленном на выявление характерных клинических и пальпаторных признаков, УЗИ щитовидной железы, исследовании антител к ткани щитовидной железы, пункционной биопсии щитовидной железы, определении функционального состояния щитовидной железы.
При ультразвуковом исследовании возможно выявление как минимальных диагностических признаков (мелких гипоэхогенных фокусов на изоэхогенном фоне), так и классической УЗ-картины АИТ – диффузного снижения эхогенности тиреоидной ткани или диффузно-неоднородной структуры.
С целью наиболее точной ультразвуковой оценки щитовидной железы при подозрении на АИТ у детей желательно проводить комплексное УЗ-исследование, включающее эховолюмометрию, эхотомографию, эходенситометрию (ЭДМ), цветовое доопплеровское картирование (ЦДК) и импульсную допплерометрию (ИДМ).
Эховолюмометрия позволяет определить тиреоидный объем, эхотомография – оценить расположение, контуры, структуру и эхогенность ткани железы, эходенситометрия выполняется для количественной оценки эхоплотности исследуемой ткани.
Цветное допплеровское картирование позволяет уточнить степень васкуляризации долей щитовидной железы, а импульсная допплерометрия – количественно оценить динамические параметры кровотока в верхней и нижней тиреоидных артериях с обеих сторон [15, 16].
- У детей с АИТ прогрессирование изменений структуры и плотности тиреоидной ткани от малоизмененной до резко измененной картины сопровождается нарастанием объема зоба, параллельным снижением эхогенности, нарушением скорости кровотока в тиреоидных артериях [15, 16].
- Обязательным методом исследования при подозрении на АИТ у детей является также определение наличия в сыворотке крови аутоантител к тиреоглобулину и микросомальному антигену в дигностически значимых титрах.
- Особенностью начальной стадии АИТ у детей является высокая частота серонегативных случаев, когда антитела к тиреоглобулину и микросомальному антигену почти у 60% больных отсутствуют [15].
- При наличии у ребенка характерной для АИТ эхографической картины и диагностически значимых титров антитиреоидных антител в сыворотке крови алгоритм обследования включает дальнейшее исследование тиреоидной функции, пункционную биопсию щитовидной железы можно не проводить.
При отсутствии у пациента типичных изменений эхогенности и эхоструктуры щитовидной железы, низком титре антитиреоидных антител или их отсутствии проводится тонкоигольная биопсия щитовидной железы.
Подтверждением аутоиммунного характера патологического процесса является инфильтрация тиреоидной ткани как зрелыми, так и молодыми лимфоцитами.
Присутствие плазматических клеток, оксифильных клеток Ашкенази также подтверждает диагноз [8, 12].
Каждому ребенку с АИТ обязательно исследуется функциональное состояние щитовидной железы, т.е. определяется уровень тиреоидных гормонов и ТТГ.
Основные принципы терапии АИТ у детей
Лечение АИТ у детей предусматривает в первую очередь консервативную медикаментозную терапию. Препаратом выбора при терапии АИТ является синтетический аналог гормона щитовидной железы L-тироксин.
При эутиреоидном состоянии и гипотиреозе L-тироксин назначается детям в максимально переносимых дозах из расчета 2,6-3,0 мкг/кг в сутки на длительный срок, каждые 3-6 месяцев проводится контроль УЗИ щитовидной железы, по показаниям назначается динамическое исследование уровней тиреоидных гормонов и ТТГ, титра антитиреоидных антител.
Обычно уже через 3 месяца от начала лечения L-тироксином у детей с АИТ отмечается выраженное уменьшение относительного объема щитовидной железы, прогрессирующее к концу 6-го месяца. При условии адекватности дозы L-тироксина и раннем начале лечения уже через полгода регулярного приема препарата объем щитовидной железы полностью нормализуется у 60% детей, больных АИТ [16].
Основанием для назначения L-тироксина детям с АИТ в стадии эутиреоза также является то, что препараты тиреоидных гормонов не только способствуют уменьшению или нормализации объема щитовидной железы и компенсируют снижение ее функции, но и препятствуют прогрессированию аутоиммунного процесса. Они тормозят секрецию ТТГ гипофизом, снижая тем самым высвобождение антигенов из щитовидной железы. Блокирование даже умеренной избыточной секреции ТТГ приводит к обратному развитию зоба [5].
Адекватность заместительной терапии L-тироксином при гипотиреозе оценивается прежде всего по уровню ТТГ, который должен быть в пределах нормальных значений. Первый контроль уровня ТТГ рекомендуется проводить не ранее, чем через 2 месяца от начала терапии. Как при явном, так и субклиническом гипотиреозе рекомендуется пожизненная заместительная терапия L-тироксином [5, 11].
На стадии гипертиреоза при АИТ возможно ограничиться симптоматическими препаратами (b-адреноблокаторы, седативные средства).
Однако на практике гипертиреоидная фаза АИТ как у взрослых, так и у детей часто расценивается как манифестация диффузного токсического зоба (ДТЗ), что объяснимо трудностями дифференциальной диагностики этих заболеваний.
В таких случаях больным проводится консервативное лечение тиреостатиками (тиамазол), доза которых, как правило, не превышает 15-20 мг в сутки.
Обычно для компенсации функции щитовидной железы при гипертиреоидной стадии АИТ достаточно проведение более коротких курсов тиреостатической терапии, чем при ДТЗ. В дальнейшем прогрессирование патологического процесса в щитовидной железе при АИТ приводит к переходу функционального состояния железы в фазу эутиреоза либо субклинического или явного гипотиреоза, что требует назначения заместительной терапии L-тироксином.
При формах АИТ, сопровождающихся наличием узлов в ткани щитовидной железы, в первую очередь решается вопрос об оперативном вмешательстве и его объеме.
Только при условии малых размеров узлов и отсутствии усиления кровотока в сосудах щитовидной железы по данным цветной допплерографии при АИТ у детей возможна консервативная терапия после обязательного проведения тонкоигольной пункционной биопсии и исключения рака щитовидной железы [4]. В таких случаях детям назначается L-тироксин в максимально переносимых дозах, что как правило составляет не менее 2,5 мкг/кг в сутки. Прогрессирование размеров узла щитовидной железы у ребенка с АИТ на фоне консервативной терапии препаратами тиреоидных гормонов является основанием для немедленного направления такого больного к хирургу.
Литература
Источник: https://www.rmj.ru/articles/obshchie-stati/Autoimmunnyy_tireoidit_u_detey/