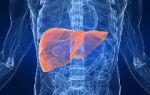
Гемохроматоз печени – это генетическое аутосомно-рецессивное заболевание, характеризующееся повышенным всасыванием и отложением железа в печени и других паренхиматозных органах. В клинике превалирует триада признаков: цирроз, гиперпигментация кожных покровов, эндокринные нарушения. Диагностика основана на изучении семейного анамнеза, выявлении нарушений обмена железа, МРТ печени с последующей биопсией, выявлении гомозиготного носительства гена гемохроматоза. Специфическое лечение включает назначение препаратов, выводящих излишки железа из организма, эфферентные методики – кровопускание, цитаферез. Заболевание неизлечимо.
Гемохроматоз печени – наследственное заболевание, при котором происходит нарушение метаболизма железа в организме, его избыточное отложение в органах и тканях.
Несмотря на системный характер нарушений, наиболее тяжело при гемохроматозе поражается печень – в ней развиваются цирротические изменения.
Отложение железа в коже проявляется гиперпигментацией, в железах внутренней секреции – эндокринными нарушениями, сахарным диабетом.
Впервые патология была описана в 1871 г., с тех пор исследования в этой области не прекращаются. На сегодняшний день выявлен ген, отвечающий за развитие гемохроматоза, связанный с HLA-комплексом гистосовместимости.
Ген этот рецессивный, поэтому для появления клиники гемохроматоза необходимо наличие данной мутации у обоих родителей пациента. Гемохроматоз печени – заболевание редкое, гетерозиготное носительство встречается у 10% населения, а гомозиготность – лишь в 0,3%.
Мужчины страдают в десять раз чаще женщин.
Гемохромaтоз печени
Генетическая природа гемохроматоза печени и его тесная связь с HLA-комплексом гистосовместимости была доказана в 1976 году. В настоящее время ученым практически удалось выделить ген, отвечающий за развитие данного заболевания.
Носительство гена может быть гомозиготным, при котором отмечается развернутая клиническая картина, и гетерозиготным.
У носителей гетерозиготных генов обычно выявляется небольшое повышение уровня железа в крови, однако излишнего отложения в тканях, а значит и клинических проявлений, не возникает.
В норме утилизация железа организмом регулируется потребностями тканей в этом микроэлементе. Железо всасывается в начальных отделах тонкой кишки и связывается в крови с транспортным белком трансферрином.
По мере необходимости железо поступает в ткани и там используется либо откладывается в связанной форме, в виде ферритина. Самые емкие депо железа – эритроциты, печень и мышцы. С течением времени ферритин в тканях начинает разрушаться с образованием пигмента гемосидерина.
Не менее трети всех запасов железа хранится в виде гемосидерина, его количество повышается при нарушениях обмена железа.
В организме здорового человека в среднем содержится примерно 4 г железа.
С пищей ежедневно поступает около 10-20 г железа, но потребляется из них не более десятой части, причем при необходимости перенос железа внутрь клеток может производиться даже против градиента концентрации.
При полном заполнении депо железа данный элемент практически прекращает всасываться в кишечнике, а при его недостатке скорость всасывания возрастает в десятки раз.
При мутации гена гемохроматоза печени поломка в ферментной системе приводит к формированию ложного сигнала о низком уровне железа в организме. Ионы этого металла начинают всасываться в повышенном количестве, что в результате приводит к накоплению не менее чем 1 г излишков железа в год.
После того, как весь пул железосвязывающих белков будет связан с металлом, железо, как сильный элемент, активирует окислительные процессы в клетке.
Это приводит к образованию большого количества свободных радикалов, а те, в свою очередь, вызывают некроз клеток, повышенный синтез коллагена, раковое перерождение тканей.
Для появления первых симптомов обычно требуется не менее 20 лет, пока общее содержание железа в организме не превысит 20-40 г.
На начальном этапе заболевания, даже при наличии генетической предрасположенности, перегрузки организма железом не наблюдается.
Следующим этапом является перегрузка тканей ионами железа без клинических проявлений. И только на поздней стадии появляются типичные клинические признаки.
Первыми проявлениями гемохроматоза печени на протяжении долгих лет могут служить лишь слабость, повышенная утомляемость, снижение половой функции у мужчин (снижение либидо и т. п.) и аменорея у женщин.
Нарушение обмена железа приводит к кальцинозу суставов, трофическим изменениям в коже и хрящах, половых органах.
На более поздних стадиях заболевания клиническая картина становится развернутой: отложение гемосидерина в коже сопровождается гиперпигментацией открытых мест, подмышечных впадин и промежности.
Из внутренних органов первой поражается печень: происходит некроз гепатоцитов, избыточное образование коллагена, что в будущем приводит к циррозу. Изначально печень увеличивается в размерах, становится плотной, болезненной при пальпации.
Затем орган уменьшается, развивается симптоматика печеночно-клеточной недостаточности и портальной гипертензии. Более чем у 80% пациентов отмечаются эндокринопатии: поражаются гипофиз и эпифиз, щитовидная, поджелудочная и половые железы.
Практически у всех больных с эндокринопатиями развивается сахарный диабет, зачастую инсулинозависимый.
Очень часто в процесс вовлекаются суставы, центральная нервная система. Отложение гемосидерина в сердце отмечается у 90-100% пациентов, но клиническая симптоматика возникает не более чем у трети больных. Гемохроматоз сердца проявляется кардиомиопатией, гипертрофией миокарда, тяжелой сердечной недостаточностью.
Консультация гепатолога необходима не только для оценки клинических данных, но также для подробного разбора семейного анамнеза, выявления наследственного характера заболевания.
Если в ходе осмотра и беседы с пациентом возникает подозрение на гемохроматоз печени, назначается ряд дополнительных анализов и консультация генетика.
УЗИ гепатобилиарной системы при гемохроматозе печени позволяет выявить значительное повышение эхогенности печеночной ткани за счет отложений гемосидерина.
Аналогичные изменения можно обнаружить и в других органах при проведении ультрасонографии поджелудочной железы, УЗИ щитовидной железы, ЭхоКГ.
Если предварительный диагноз подтверждается с помощью МРТ печени, то пациент направляется на пункционную биопсию печени с последующим морфологическим исследованием биоптатов.
Абсолютным доказательством правомочности диагноза является обнаружение дефектного гена гемохроматоза печени при кариотипировании.
КТ органов брюшной полости. Диффузное повышение плотности печени до 80 ед. Хаунсфилда (преконтрастное изображение) за счет диффузного отложения железа.
Методов полного излечения патологии в современной гастроэнтерологии не существует, поэтому терапия направлена на купирование симптомов заболевания. Для начала назначается диета с пониженным содержанием железа и повышенным уровнем белка.
В последующем используются методики, позволяющие усилить выведение железа из организма. Наиболее доступный способ уменьшить пул железа – кровопускание. Для правильного расчета объема кровопускания учитываются уровни гемоглобина, гематокрита, трансферрина.
При заборе 500 мл крови теряется 200-250 мг железа. В среднем производится эксфузия 300 мл крови дважды в неделю.
Более сложным методом, требующим специального оборудования, является цитаферез – при этом осуществляется удаление клеточных элементов, а плазма возвращается в кровяное русло. Сеансы кровопусканий или цитафереза проводятся до развития умеренной анемии.
Так как на фоне исходной анемии использование эфферентных методик ограничено, то в качестве подготовки и сопровождения цитафереза назначается рекомбинантный эритропоэтин. Данный препарат усиливает утилизацию железа, благодаря чему снижается его концентрация в тканях, повышается гемоглобин.
Курс введения эритропоэтина – 10-15 недель.
Другим методом лечения гемохроматоза печени является использование дефероксамина – 500 мг этого препарата выводит из организма почти 45 мг железа. Курс лечения дефероксамином составляет не менее 30-40 дней. Одновременно проводят симптоматическую терапию цирроза печени, сердечной и печеночной недостаточности, сахарного диабета.
Течение заболевания длительное, а прогноз благоприятный лишь при своевременном начале лечения.
Если патогенетическая терапия была инициирована до значительной перегрузки организма железом, развития цирроза, диабета и полиорганной недостаточности — выживаемость увеличивается на несколько десятилетий.
В случае развития цирроза риск гепатоцеллюлярной карциномы возрастает в 200 раз. Смерть обычно наступает от печеночной недостаточности и ее осложнений. Профилактика не разработана.
Источник: https://www.KrasotaiMedicina.ru/diseases/zabolevanija_gastroenterologia/hepatic-hemochromatosis
Гемохроматоз печени — причины, симптомы, диагностика и лечение у мужчин и женщин, диета
Гемохроматоз печени (бронзовый диабет, пигментный цирроз) — заболевание, связанное с нарушением усвоения железа в организме.
Первые признаки у большинства заболевших проявляются после достижения 40-летнего возраста. Чаще всего встречается наследственный гемохроматоз (3-4 случая на 1000 больных).
При отсутствии своевременного грамотного лечения болезнь приводит к развитию тяжёлых осложнений, в том числе и рака печени.
Что такое г емохроматоз
Гемохроматоз печени является одной из наиболее распространённых наследственных болезней. Его код в МКБ-10 — E83. 1 (нарушения обмена железа).
Гемохроматоз также именуют бронзовым диабетом, поскольку генетические клетки при этом заболевании работают так, что человеческий организм всасывает железо в избыточном количестве, не позволяя клеткам своевременно избавляться от его излишков. Это провоцирует накопление пигментов и железосодержащих элементов во внутренних органах, что приводит к появлению характерной окраски кожи и органов. При избыточном количестве железа в тканях клетки гибнут.
Это заболевание развивается чаще всего у мужчин, а женщины страдают им в три раза реже.
Специалисты выделяют две формы гемохроматоза: первичную и вторичную. Первичная форма встречается чаще и является наследственной, связанной с генным дефектом. В этом случае бронзовый диабет развивается в основном у людей, получивших дефектный ген от матери и отца.
Первичная форма делится на несколько типов:
- аутосомно-рецессивный классический;
- ювенильный;
- аутосомно-доминантный;
- наследственный неассоциированный.
Вторичная форма бронзового диабета развивается из-за приобретённой дисфункции систем, принимающих участие в процессе обмена железа, и встречается в редких случаях. Она также делится на следующие типы:
- алиментарный;
- метаболический;
- неонатальный;
- посттрансфузионный;
- смешанный.
Неонатальный гемохроматоз развивается только у новорожденных. При этом основные симптомы заболевания проявляются в первые часы после рождения.
В группе риска находятся недоношенные мальчики, у которых болезнь встречается в два раза чаще, чем у девочек.
Медикаментозное лечение в таких случаях не приносит желаемых результатов, и для спасения жизни ребёнка прибегают к пересадке печени.
Причины развития
Наследственный или первичный бронзовый диабет может развиваться из-за мутации гена, находящегося в 4-й хромосоме, левом плече. Причин возникновения вторичной формы гораздо больше и чаще всего провоцируют появление гемохроматоза следующие заболевания:
- талассемия;
- алкогольный цирроз печени;
- гепатит;
- анемия;
- рак печени;
- кожная порфирия.
Вторичная форма также может развиться после переливания, поскольку донорская кровь содержит чужеродные красные кровяные тельца, погибающие раньше собственных и выделяющие железо. Среди прочих причин возникновения бронзового диабета стоит выделить и чрезмерный приём железосодержащих препаратов и соблюдение низкобелковой диеты.
Симптомы и стадии
Первые признаки гемохроматоза появляются, когда в организме человека накапливается до 40 г железа. Наиболее явным симптомом этого заболевания является пигментация. Кожа на лице, шее, руках, половых органах и подмышках пациента приобретает сероватый и бронзовый оттенок. При этом яркость этого признака зависит от давности течения гемохроматоза.
Яркий признак гемохроматоза — бронзовый оттенок кожи
Появление характерных признаков бронзового диабета зависит не только от стадии заболевания, но и от пола пациента. Так, у мужчин изначально наблюдаются атрофические изменения яичек и снижение потенции. По мере развития гемохроматоза возникает полная импотенция и гинекомастия (увеличение в объёме и рост молочных желез).
У женщин на развернутой стадии бронзового диабета нередко диагностируют бесплодие и аменорею (отсутствие менструаций в течение полугода и более ).
Диагностика
При обнаружении характерных симптомов бронзового диабета следует сразу же записаться на приём к гепатологу. Для подтверждения диагноза в клинике проведут визуальный осмотр и назначат ряд следующих процедур:
- Анализ мочи, крови. Они необходимы для выявления уровня железа, белков и ферментов в организме, обнаружения инфекции и воспаления.
- УЗИ поражённых органов. Ультразвуковое исследование помогает оценить состояние сердца, печени и кишечника.
- МРТ. Во время этой процедуры исследуется состояние печени и степень поражения её тканей.
- Генетическое тестирование. Оно требуется для определения наличия дефектного гена в организме.
- Биопсия. В ходе процедуры изучается фрагмент печени на предмет цирроза и злокачественных новообразований.
При подозрении на развитие осложнений дополнительно назначается рентгенография суставов и определение уровня сахара в крови.
Методы лечения
После подтверждения диагноза врач разработает схему лечения. Вне зависимости от формы бронзового диабета терапия бывает комплексной и включает в себя:
- приём лекарственных препаратов;
- соблюдение специальной диеты;
- использование средств народной медицины.
При лечении гемохроматоза нередко применяется и такая процедура, как кровопускание. Она необходима для выведения из организма крови с избыточным содержанием железа. В запущенных случаях врач принимает решение прибегнуть к оперативному вмешательству.
Медикаментозное лечение бронзового диабета направлено на уменьшение количества железа в печени, восстановление тканей этого внутреннего органа и устранение причины развития болезни. Специалисты чаще всего назначают препараты, относящиеся к следующим группам лекарственных средств:
- Хелаторы. Лекарства направлены на выведение железа из печени. Чаще всего при бронзовом диабете назначают Дефероксамин.
- Гепатопротекторы. Медикаменты улучшают состояние поражённого органа и нормализуют его работу.
Использование лекарственных средств из других групп зависит от состояния пациента. В некоторых случаях специалист дополнительно назначает антибактериальную терапию и приём лекарств, направленных на улучшение работы сердца и повышение иммунитета.
Продолжительность применения любых медикаментозных средств и их дозировку определяет лечащий врач.
Соблюдение диеты
Большинство железосодержащих продуктов придётся исключить из рациона
Важную роль в лечении бронзового диабета играет диетотерапия, подразумевающая исключение из рациона продуктов с повышенным содержанием железа. К этой группе относятся:
- свинина и говядина (чем темнее мясо, тем больше в нём содержится железа);
- морепродукты;
- гречка;
- фисташки;
- яблоки;
- шпинат;
- бобовые;
- петрушка;
- кукуруза.
На время лечения также следует отказаться от употребления алкоголя, яиц и блюд с повышенным содержанием витамина C, который способствует накоплению железа. При гемохроматозе рекомендуется пить кофе и черный чай, поскольку эти напитки снижают количество микроэлемента в организме.
Использование народных средств
В качестве дополнительной терапии используются средства народной медицины. Наиболее эффективны при лечении бронзового диабета следующие:
Перед применением средств народной медицины следует проконсультироваться с лечащим врачом.
Хирургическое вмешательство
Кардинальным методом лечения бронзового диабета является оперативное вмешательство. К нему врач прибегает в том случае, если у пациента диагностирован цирроз печени или поражение суставов. При нарушении подвижности больному показана операция по установке протеза.
При прогрессирующем циррозе требуется пересадка поражённого органа, необходимая для сохранения жизни больному. Хирургическое вмешательство осуществляется под общим наркозом после соблюдения определённых условий по подготовке.
Своевременное лечение поможет избежать возникновения серьезных осложнений. Нарушения в организме происходят в запущенных случаях, и у пациента развиваются следующие заболевания:
- печёночная недостаточность;
- инфаркт;
- рак печени;
- сахарный диабет;
- цирроз печени;
- суставные заболевания;
- аритмия.
При отсутствии квалифицированной помощи пациент погибает от перитонита, печёночной или диабетической комы.
Меры профилактики
Профилактика гемохроматоза включает в себя соблюдение следующих общих рекомендаций:
- отказ от приёма медикаментов, повышающих гемоглобин;
- исключение из рациона продуктов с высоким содержанием железа;
- употребление белковой пищи.
Если у одного или обоих родителей диагностирован гемохроматоз, детям необходимо регулярно сдавать кровь на контроль уровня железа в организме и проходить обследование в клинике.
Если лечение гемохроматоза начато сразу же после обнаружения характерных симптомов, то развития осложнений можно избежать, а прогноз будет благоприятным.
При игнорировании признаков заболевания состояние больного стремительно ухудшается, а продолжительность его жизни значительно сокращается. Из-за нарушения обмена веществ в организме у пациента развиваются заболевания, несовместимые с жизнью.
На начальной стадии бронзовый диабет хорошо поддаётся комплексному лечению, а больному не требуется хирургического вмешательства.
Источник: https://medknsltant.com/gemohromatoz/
Что такое гемохроматоз печени
Сегодня среди патологических заболеваний печени выявлено множество болезней, несущих генетическую предрасположенность.
Причинами таких заболеваний могут быть различные факторы, способствующие изменению нормального генетического кода в патологическую сторону, вследствие чего возникают нарушения работы той или иной системы.
К таким заболеваниям печени относится и гемохроматоз печени, разговор о котором пойдет в данной статье.
Гемохроматоз печени – это наследственная патология
Причины
Для того чтобы ответить на вопрос, какие причины и факторы становятся следствием возникновения болезни, необходимо выяснить, что такое гемохроматоз и какова сущность его происхождения.
Гемохроматоз – это наследственная патология, связанная с нарушением выработки железа в организме и отложением его в избытке в различных органах и тканях.
Такое заболевание часто называют бронзовым диабетом, потому что при этом генетические клетки работают таким образом, что организм человека в больших количествах всасывает ферменты железа, не позволяя клеткам вовремя избавляться от его избытков.
Гемохроматоз печени делится на первичный и вторичный, что обусловлено появлением и проявлением этой болезни в течение жизни пациента. Кроме того, сегодня выделяют еще одну форму гемохроматоза, появляющегося у новорождённых детей. Причины такой формы до сих пор не выяснены.
Первичный гемохроматоз печени – это редкая, имеющая чисто генетический характер, патология.
Причина такого недуга связана с нарушением рецессивного гена клеток, вследствие чего организм не может перерабатывать железо, поглощая и впитывая его в ткани в больших количествах.
Такое заболевание носит название идиопатического гемохроматоза, поскольку отложения железа происходят во многих органах, в основном – кишечнике, печени и поджелудочной железы.
Со временем, чем больше металла накапливается в органах, тем хуже начинают функционировать ткани. Впоследствии, органы могут отказать полностью и привести к смерти пациента, если вовремя не предпринять меры по очистке и выведению накопившегося вещества.
Вторичный гемохроматоз – это достаточно редкое проявление нарушений функций печени, которое развивается и связано с воздействием на орган каких-либо факторов, или заболеваний.
Обычно толчком для развития этого заболевания является цирроз печени, который влечёт за собой нарушение функций органа, а именно повышенный уровень трансферрина – вещества, отвечающего за транспортировку и переработку железа в организме.
Вследствие того, что переносить железо по органам становится нечему, оно начинает в больших количествах откладываться в самой печени.
Кроме того, фактором, являющимся следствием развития патологии может быть и злоупотребление алкогольными напитками, которые не дают клеткам печени и тонкого кишечника перерабатывать излишки минерала в организме, вызывая наследственный гемохроматоз. Многократное переливание крови или гемодиализ также способствуют развитию болезни.
Симптомы
Гемохроматоз или пигментный цирроз печени – патология, проявляющая себя через определённый промежуток времени. Для появления первичных клинических проявлений может пройти несколько десятков лет – это зависит от того, как быстро будет накапливаться железо в организме.
Важно понимать, симптоматика болезни напрямую связана с тем, в каком органе откладывалось вещество. Так, в случае нарушения функции печени, гемохроматоз будет иметь клинические проявления, причины которой зависят от стадии развития болезни и степени:
Появление пигментации на определённых участках тела — частый симптом гемохроматоза
- Появление пигментации на определённых участках тела – обычно такое проявление начинается на животе, лице, запястьях и наружных половых органах. Это очень частый симптом, который возникает практически у всех больных.
- Выпадение волос на туловище и лице.
- Болезненность в брюшной полости, которая носит генерализованный характер и не имеет чёткой локализации.
- Нарушения работы органов ЖКТ – тошнота, рвота, нарушения стула, анорексические проявления.
- Увеличение размеров печени.
- Уменьшение сексуальной активности у мужчин и ранняя менопауза у женщин.
- Появления признаков цирроза печени.
- Портальная гипертензия.
Развитие этой симптоматики несёт постепенный характер, что связано с постепенным накапливанием вещества в клетках. Обычно, симптомы проявляются к 40-45 годам.
Диагностика
Для постановки диагноза гемохроматоз проводят тщательную диагностику, поскольку эта патология по симптоматике схожа со многими заболеваниями органов брюшины. Диагностические процедуры, связанные с распознаванием болезни имеют строгую поэтапность, необходимую для тщательного сбора данных и исследований.
Начальным этапом диагностики является выявление анамнеза жизни пациента и его родственников – проявление патологий в наследственности. Для этого проводят сбор жалоб и опрос пациента, его родственников и тщательно изучают генетическую предрасположенность больного к заболеванию.
Вторым этапом диагностики гемохроматоза являются лабораторные исследования крови и мочи, включающие в себя:
- Анализы крови. В случае, если у пациента заподозрена патология, обычно в крови обнаруживается повышение уровня железа в сыворотке и трансферрина – вещества, отвечающего за транспорт железа в организме. При повышении показателей выше допустимой нормы, врачи вправе задуматься о присутствии в организме скоплений вещества.
- Общий и биохимический анализ мочи, при наличии болезни, также выявит повышение уровня вещества в выделяемой жидкости.
- Генетический ДНК тест – это специальный тест, исследующий клетки пациента на элемент присутствия в них отклонений.
- Биопсия– метод, позволяющий выявить нарушение и поражение тканей органа. При этом проводится стернальная пункция и пункция кожи, которые при патологии будут содержать большое количество меланина и железа.
Третий шаг в подтверждении диагноза гидрохроматоза является так называемое кровопускание – флеботомия. Его суть заключается в том, что через определённые промежутки времени пациенту делают небольшой прокол и выпускают некоторое количество крови. если состояние больного улучшилось – значит диагноз подтверждается практически 100%.
Основную сложность в постановке диагноза составляет неонатальный гемохроматоз, поскольку до сих пор не выяснено причин его возникновения.
В данном случае, при появлении признаков заболевания у ребёнка проводят биохимию и анализ крови, а также используют дополнительные методы – рентгенографию и УЗИ органов брюшины.
Кроме того, детей и родителей, которые генетически предрасположены к этому недугу,отправляют на консультацию с генетиками.
Лечение
Важно понимать, что полностью излечиться от данного заболевания невозможно, поскольку это генетическое отклонение, а значит, избавиться от причины патологии не представляется возможным.
При гемохроматозе нельзя есть продукты с железом, например, мясо
Терапия гемохроматоза направлена в первую очередь на снижение симптоматики и облегчение состояния пациента. Для этого разработаны целые комплексы процедур, включающие в себя диетическое питание, фильтрацию и очистку крови, лекарственную терапию и некоторые хирургические процедуры.
Диетотерапия при гемохроматозе включает в себя ряд продуктов, содержащих в своем составе минимальное или полное отсутствие железа. Так, пациент должен полностью устранить из рациона мясные блюда, алкогольные напитки, морепродукты.
Кроме того, диета при патологии подразумевает и ограничение блюд, содержащих витамин С, поскольку это вещество усиливает всасывание железа и способствует еще большему накоплению его в организме больного.
А вот чёрный чай и кофе, напротив, будут полезны при данном заболевании, потому что они снижают переработку железосодержащих веществ.
К основным методам поддерживающей терапии болезни относится кровопускание, которое позволяет облегчить состояние пациента и снизить уровень железа в крови. Также на фоне данной процедуры целесообразно назначение средств, влияющих на вывод железа из организма.
Осложнения и прогноз
Своевременная диагностика и поддерживающая терапия позволяют устранить основные проявления патологии. Однако в запущенных случаях могут быть последствия, такие как:
- Нарушения работы сердечной системы – инфаркты, аритмии, ИБС.
- Развитие печёночной недостаточности.
- Сосудистые кровотечения.
- Опухоли печени.
- Кома печени и диабетическая кома.
- Болезни суставов.
- Снижение половой активности.
- Септические осложнения.
Прогноз заболевания зависит от качества проводимой диагностики и лечения, а также от уровня и скорости накопления железа в организме. Так, в случае своевременной диагностики, прогноз может быть благоприятный, однако, более 50% случаев гемохроматоз печени дают осложнения и пациенты погибают, поскольку провести профилактику этой болезни невозможно.
Видео
Гемохроматоз. Симтомы, причины и методы лечения.
Источник: https://pechen.org/bolezni/chto-takoe-gemohromatoz-pecheni.html
Гемохроматоз
Любые заболевания печени проводят к дисфункции других органов и систем организма. Ведь печень — фильтр организма, который освобождает его от токсинов, тяжелых металлов, избытка гормонов, жира.
Гемохроматоз — заболевание печени наследственного характера. Такой генетический сбой провоцирует повышение всасывания железа в органах пищеварительной системы, крови. Так, наблюдается излишнее скопление железа в тканях и органах.
Что такое гемохроматоз, каковы его признаки? И как лечить такое тяжелое заболевание?
Что такое гемохроматоз?
Гемохроматозом называется заболевание печени, которое характеризуется нарушением обмена железа. Это провоцирует к накоплению железосодержащих элементов и пигментов в органах. В дальнейшем такое явление приводит к возникновению полиорганной недостаточности. Свое название заболевание получило из-за характерного окраса как кожных покровов, так и внутренних органов.
Очень часто встречается именно наследственный гемохроматоз. Его частота составляет около 3-4 случаев на 1000 человек населения. При этом, гемохроматоз чаще встречается у мужчин, нежели у женщин.
Активное развитие, и первые признаки недуга начинают себя проявлять в возрасте 40-50 лет.
Так как гемохроматоз поражает практически все системы и органы, лечением заболевания занимаются врачи разных направлений: кардиология, гастроэнтерология, ревматология, эндокринология.
Специалисты различают два основных типа недуга: первичный и вторичный. Первичный гемохроматоз — дефект ферментных систем. Данный дефект провоцирует накопление железа во внутренних органах. В свою очередь, первичный гемохроматоз делится на 4 формы, в зависимости от дефективного гена:
- Аутосомно-рецессивный классический;
- Ювенильный;
- Наследственный неассоциированный;
- Аутосомно-доминантный.
Развитие вторичного гемохроматоза происходит на фоне приобретенной дисфункции ферментных систем, которые принимают участие в процессе обмена железа.
Вторичный гемохроматоз тоже делится на несколько типов: алименарный, посттрансфузионный, метаболический, неонатальный, смешанный.
Развитие любой формы гемохроматоза происходит в 3 этапа — без избытка железа, с избытком железа (без симптоматики), с избытком железа (с проявлением яркой симптоматики).
Основные причины гемохроматоза
Наследственный гемохроматоз (первичный) — болезнь аутосомно-рецессивного типа передачи. Основной причиной такой формы можно назвать мутацию гена, который называется HFE. Он находится на коротком плече в шестой хромосоме.
Мутации данного гена провоцируют нарушения захвата железа клетками кишечника. В результате этого формируется ложный сигнал о нехватке железа в организме и крови. Такое нарушение ставится причиной повышенного выделения белка DCT-1, который связывает железо.
Следовательно, абсорбция элемента в кишечнике усиливается.
Далее, патология приводит к избытку пигмента железа в тканях. Как только возникает избыток пигмента, наблюдается гибель многих активных элементов, что становится причиной склеротических процессов. Причиной появления вторичного гемохроматоза является излишнее поступление железа в организм извне. Данное состояние нередко возникает на фоне следующих проблем:
- Чрезмерный прием препаратов с железом;
- Талассемия;
- Анемия;
- Кожная порфирия;
- Алкогольный цирроз печени;
- Вирусные гепатиты В, С;
- Злокачественные опухоли;
- Соблюдение низкобелковой диеты.
Симптоматика заболевания
Гемохроматоз печени характеризуется яркой симптоматикой. Но, первые признаки недуга начинают проявлять себя в зрелом возрасте — после 40 лет. Именно к этому периоду жизни в организме скапливается до 40 граммов железа, что значительно превышает все допустимые нормы. В зависимости от этапа развития гемохроматоза различают и симптомы заболевания. Стоит рассмотреть их более подробно.
Симптомы начальной стадии развития
Заболевание развивается постепенно. На начальном этапе симптоматика не выражена.
В течение многих лет больной может жаловаться на общую симптоматику: недомогание, слабость, повышенная утомляемость, снижение массы тела, снижение потенции у мужчин.
Далее, к этим признакам начинают присоединяться и более выраженные признаки: болевой синдром в области печени, боль в суставах, сухость кожных покровов, атрофические изменения яичек у мужчин. После этого возникает активное развитие гемохроматоза.
Признаки развернутой стадии гемохроматоза
Основными признаками данной стадии являются следующие осложнения:
- Пигментация кожных покровов;
- Пигментация слизистых оболочек;
- Цирроз печени;
- Сахарный диабет.
Наследственный гемохроматоз, как и любая другая форма, характеризуется пигментацией. Это самый частые и основной признак перехода недуга в развернутую стадию.
Яркость симптома зависит от давности течения заболевания. Дымчатый и бронзовый оттенок кожи, чаще всего проявляется на открытых участках кожи — лице, руках, шее.
Также, характерная пигментация наблюдается на половых органах, в подмышечных впадинах.
Избыток железа, в первую очередь откладывается именно в печени. Поэтому, почти у каждого больного при диагностике фиксируется увеличение железы. Меняется и структура печени — она становится более плотной, болезненной при пальпации. У 80% больных развивается сахарный диабет, и в большинстве случаев он инсулинозависимый. Эндокринные изменения проявляются и в таких признаках:
- Дисфункция гипофиза;
- Гипофункция эпифиза;
- Нарушение работы надпочечников;
- Дисфункция половых желез, щитовидной железы.
Излишнее накопление железа в органах сердечно-сосудистой системы при первичном наследственном гемохроматозе происходит в 95% случаев. Но, симптоматика со стороны работы сердца проявляется только в 30% всех случаев заболевания.
Так, диагностируется увеличение сердца, аритмия, рефрактерная сердечная недостаточность. Есть характерные симптомы в зависимости от пола. Так, мужчин наблюдается атрофия яичек, полная импотенция, гинекомастия.
У женщин часто возникает бесплодие, аменорея.
Симптоматика термальной стадии гемохроматоза
В этот период специалисты наблюдают процесс декомпенсации органов. Проявляется это в виде развития портальной гипертензии, печеночной недостаточности, желудочковой сердечной недостаточности, истощения, дистрофии, комы диабетической.
В таких случаях смертность наступает, чаще всего, от кровотечения расширенных варикозных вен пищевода, перитонита, диабетической и печеночной комы. Возрастает риск развития опухолевых новообразований.
Редкой формой считается ювенильный гемохроматоз, который активно развивается в возрасте 20-30 лет. В основном, поражаются печень и сердечная система.
Диагностика гемохроматоза
Диагностика проводится специалистом, в зависимости от основного симптома. Так, пациент может обратиться за помощью к кардиологу, гастроэнтерологу, гинекологу, эндокринологу, ревматологу, урологу или дерматологу.
При этом, варианты диагностики одинаковы, независимо от клинических проявлений гемохроматоза.
После проведения первичного осмотра, сбора анамнеза, жалоб пациента назначаются лабораторные и инструментальные исследования, которые позволят подтвердить или опровергнуть диагноз.
По результатам лабораторных исследований можно будет поставить точный диагноз. Так, на наличие гемохроматоза будут указывать следующие показатели:
- Высокий уровень железа в крови;
- Повышение уровня трансферрина и ферритина в сыворотке крови;
- Повышенное выделение железа с уриной;
- Низкая железосвязывающая способность сыворотки крови.
Далее, специалист может назначить проведение биопсии печени или кожных покровов при помощи пункции. Во взятых образцах будут обнаружены отложения гемосидерина, что тоже укажет на гемохроматоз.
Наследственный гемохроматоз устанавливается при помощи молекулярно-генетического исследования.
Для установления степени поражения, состояния пораженных внутренних органов требуется проведение инструментальной диагностики.
Наиболее популярным методом исследования является УЗИ пораженных органов. Есть возможность оценить состояние печени, сердца, кишечника. Для более детальной диагностики назначают МРТ или КТ, рентгенографию суставов. Дополнительно можно провести исследование печеночных проб, мочи, уровня сахара в крови, гликозилированного гемоглобина.
Лечение гемохроматоза
Терапия гемохроматоза проводится обязательно комплексная. Основной задачей такого лечения является выведение железа из организма. Но, очень важно, чтобы диагноз был поставлен правильно. Только после этого назначается лечение. Заниматься самолечением категорически запрещено. Итак, первым этапом терапии считается прием железосвязывающих препаратов.
Такие препараты при попадании в организм начинают активно связываться с молекулами железа, с дальнейшим их выведением. С этой целью часто используется 10-% раствор десферала. Он предназначен для внутривенного введения. Курс терапии назначается исключительно доктором, в зависимости от тяжести течения гемохроматоза. В среднем курс длится 2-3 недели.
Обязательным условием в комплексном лечении гемохроматоза является проведение флеботомии. Данная процедура еще известна под названием кровопускания. Еще с давних времен кровопусканием лечение разнообразные заболевания. А гемохроматоз отлично поддается такому варианту терапии. Благодаря пусканию уменьшается количество эритроцитов в общем количестве крови.
Следовательно, снижается и уровень железа. Помимо этого, флеботомия быстро устраняет пигментацию, дисфункции печени. Но, важно соблюдать все дозировки и правила проведения процедуры. Так, допустимым считается спуск 300-400 мл крови за раз. А вот при потере 500 мл крови у пациента может ухудшиться самочувствие. Достаточно проводить процедуру 1-2 раза в неделю.
В период лечения стоит соблюдать такие условия:
- Полное исключение алкоголя;
- Отказ от приема БАДов;
- Отказ от приема витамина С, мультивитаминных комплексов;
- Исключение из рациона питания продуктов с высоким уровнем железа;
- Отказ от употребления легкоусвояемых углеводов.
Для очищения крови, специалисты могут прибегнуть к помощи плазмафереза, цитафереза или гемосорбции. Одновременно с выведением железа стоит проводить симптоматическое лечение печени, сердечной недостаточности, сахарного диабета. Комплексное лечение заболевания включает в себя и соблюдение определенной диеты.
Диета гемохроматозе
Соблюдение диеты при таком заболевание играет важную роль в процессе лечения. Так, из рациона больного полностью исключаются продукты, которые являются источником большого количества железа. К таким можно отнести следующие:
- Свинина, говядина;
- Гречневая крупа;
- Фисташки;
- Яблоки;
- Бобы;
- Кукуруза;
- Шпинат;
- Петрушка.
Стоит помнить, что, чем темнее мясо, тем больше в нем находится данного микроэлемента. При гемохроматозе категорически запрещено употреблять любые алкогольные напитки.
К усиленному усвоению железа приводит потребление витамина С. Поэтому, аскорбиновую кислоты тоже стоит исключить. Специалисты утверждают, что не нужно полностью отказываться от продуктов, содержащих железо.
Необходимо просто минимизировать количество их потребления.
Ведь гемохроматоз — болезнь избытка железа. Стоит нормализовать его уровень. А вот дефицит железа спровоцирует тяжелые заболевания крови. Все должно быть в меру. При составлении диетического меню, нужно заменить темное мясо на светлое, гречневую кашу на пшеничную. Соблюдение такой диеты ускорит процесс выздоровления, улучшит общее состояние больного.
Каков прогноз?
В случае своевременного выявления гемохроматоза жизнь пациента продлевается на десятилетия. В целом, прогноз определяется с учетом перегрузки органов.
К тому же, гемохроматоз возникает в зрелом возрасте, когда нередко развиваются сопутствующие хронические недуги. Если не заниматься терапией гемохроматоза длительность жизни будет составлять максимум 3-5 лет.
Неблагоприятный прогноз наблюдается и в случае поражения печени, сердца и эндокринной системы при данном недуге.
Чтобы избежать развития вторичного гемохроматоза стоит следовать правилам профилактики.
Основными являются рациональное, сбалансированное питание, прием препаратов железа только под контролем врача, периодическое переливание крови, исключение алкоголя, наблюдение у рвача при наличии заболеваний сердца и печени. Первичный гемохроматоз требует семейного скрининга. После этого начинается максимально эффективное лечение.
Источник: http://vpecheni.ru/drugie-bolezni/gemohromatoz.html
Гемохромaтоз печени: причины заболевания, основные симптомы, лечение и профилактика
Представляет собой генетическое аутосомно-рецессивное заболевание, характеризующееся повышенным всасыванием и отложением железа в печени и других паренхиматозных органах.
Причины
Наследственная этиология гемохроматоза и его тесная связь с HLA-комплексом гистосовместимости была установлена в 1976 году. В наше время ученым практически удалось выделить ген, который отвечает за возникновение данного заболевания.
Носительство гена может быть гомозиготным, в этом случае отмечается развитие развернутой клинической картины, и гетерозиготным. У лиц с гетерозиготным геном чаще всего заболевание проявляется незначительным повышением уровня железа в крови, однако повышенного депонирования его в тканях.
При данной форме выраженных клинических проявлений не развивается.
В норме удаление железа с организма регулируется потребностями тканей в этом микроэлементе. Адсорбция железа происходит в начальных отделах тонкой кишки и связывается в крови с транспортным белком трансферрином.
Затем по мере необходимости железо поступает в ткани и там используется либо откладывается в связанной форме, в виде ферритина. Самые объемными депо железа, являются эритроциты, печень и мышцы. Через какое-то время ферритин в тканях начинает разрушаться с формированием пигмента гемосидерина.
Не менее трети всех запасов железа в нашем организме хранится в виде гемосидерина, при этом его количество повышается при нарушении обмена железа.
В норме в организме содержится около 4 г железа. Ежедневно с продуктами питания поступает от 10 до 20 г железа, из которых потребляется не более десятой части, причем при необходимости перенос железа внутрь клеток может производиться даже против градиента концентрации.
При полном заполнении депо железа данный элемент практически прекращает всасываться в кишечнике, а при его недостатке скорость его всасывания значительно повышается. При гемохроматозе печени поломка в ферментной системе приводит к формированию ложного сигнала, указывающего на нехватку железа в организме.
Ионы этого металла начинают всасываться в повышенном количестве, что в результате приводит к накоплению не менее чем 1г излишков железа в год. После того, как весь пул железосвязывающих белков будет связан с металлом, железо, как сильный элемент, активирует окислительные процессы в клетке.
Такие процессы вызовут образование большого количества свободных радикалов, а те, в свою очередь, вызовут некроз клеток, повышенную выработку коллагена и раковое перерождение тканей.
Симптомы
Первые симптомы гемохроматоза печени возникают как минимум через 20 лет. Заболевание может отличаться бессимптомным течением пока накопление этого элемента не достигнет 20 либо 40 г.
На начальном этапе заболевания, даже при наличии генетической предрасположенности, перегрузки организма железом не наблюдается. Следующим этапом заболевания является перегрузка тканей ионами железа без клинических проявлений.
И только на поздней стадии недуга может развиваться типичная клиническая симптоматика.
Начальными проявлениями гемохроматоза печени на протяжении долгих лет могут являться только слабость, повышенная утомляемость, снижение половой функции у мужчин и аменореи у женщин.
Нарушение обмена железа приводит к кальцинозу суставов, трофическим изменениям в коже и хрящах, половых органах.
На более поздних стадиях заболевания клиническая картина становится развернутой: отложение гемосидерина в коже сопровождается гиперпигментацией открытых мест, подмышечных впадин и промежности.
Диагностика
При подозрении на это заболевание больному проводится оценка клинических данных, изучение семейного анамнеза, выявление наследственной предрасположенности к заболеванию.
Если в ходе осмотра и беседы с пациентом возникает подозрение на гемохроматоз печени, то больному назначается консультация генетика, ультразвуковое исследование печени и щитовидной железы.
Если предварительный диагноз подтверждается с помощью магниторезонансной томографии печени, то пациент направляется на пункционную биопсию печени с последующим морфологическим исследованием биоптатов.
Лечение
На данный момент не разработано схемы лечения, позволяющей полностью избавится от заболевания.
Таким больным назначается диета с пониженным содержанием железа и повышенным уровнем белка. В дальнейшем используются методики, позволяющие усилить выведение железа из организма.
Наиболее доступный способ снизить пул железа – это кровопускание. Для правильного расчета объема кровопускания учитываются уровни гемоглобина, гематокрита, трансферрина.
Более сложным способом, требующим специального оборудования, является цитаферез, посредством метода осуществляется удаление клеточных элементов, а плазма возвращается в кровяное русло.
В некоторых случаях больному может быть назначено введение рекомбинантного эритропоэтина.
Другим методом лечения гемохроматоза печени является использование дефероксамина. Совместно с использованием лекарственного средства проводят симптоматическую терапию цирроза печени, сердечной и печеночной недостаточности, сахарного диабета.
Профилактика
На данный момент не разработано специфических методов профилактики развития гемохроматоза печени.
Источник: https://www.obozrevatel.com/health/bolezni/gemohromatoz-pecheni.htm
Гемохроматоз
Важная роль железа для организма человека установлена еще в XVIII в. Железо незаменимо в процессах кроветворения и внутриклеточного обмена.
Этот элемент входит в состав гемоглобина крови , отвечающего за транспорт кислорода и выполнение окислительных реакций.
Железо, являясь составной частью миоглобина и гемоглобина, входит в состав цитохромов и ферментов, принимающих участие в окислительно-восстановительных реакциях. Подробнее: Железо .
Нормальные запасы железа в организме составляют 300–1000 мг для взрослых женщин и 500–1500 мг для взрослых мужчин.
Суточная потребность в железе составляет 10 мг у мужчин и 20 мг у женщин. Считается, что оптимальная интенсивность поступления железа составляет 10-20 мг/сутки. Дефицит железа может развиться, если поступление этого элемента в организм будет менее 1 мг/сутки.
Количество железа в организме изменяется в зависимости от веса, концентрации гемоглобина, пола и размера депо. Самое большое депо – гемоглобин, в частности в циркулирующих эритроцитах.
Запасы железа здесь варьируют в соответствии с массой тела, полом и концентрацией гемоглобина крови и составляют примерно 57% от всего железа, содержащегося в организме человека. Например, человек, весящий 50 кг, чья концентрация гемоглобина крови – 120 г/л имеет содержание гемового железа 1,1 г.
Количества негемового запаса железа, содержащегося в форме ферритина и гемосидерина также зависит от возраста, пола, размера тела, а кроме того, от его потери (от кровотечения), беременности или перегрузки железом (при гемохроматозе). Тканевой пул железа включает миоглобин и крошечную, но эссенциальную фракцию железа в ферментах.
Примерно 9% железа содержится в в миоглобине. Существует «лабильный пул» – быстрый компонент рециркуляции, который не имеет определенного анатомического или клеточного местоположения.
Адекватные питание и терапия должна не только исправить дефицит поступления железа, но также восполнить утерянные запасы железа. Безопасное потребление железа при диетическом питании – до 45 мг/сут.
Ежедневные потери железа составляют примерно 1 мг в день. В основном они осуществляются через пищеварительный тракт: десквамация эпителиальных клеток кишечника (0,3 мг/сут), микрокровотечения и потери с желчью. Железо также теряется при десквамации эпителиальных клеток кожи и в меньшей степени с мочой (менее 0,1 мг/сут).
У здоровых людей компенсация этих потерь происходит путем абсорбции железа из пищи. Нормальный баланс железа поддерживается в значительной степени регулированием его всасывания. Поступившее неорганическое железо, солюбилизируется и ионизируется кислым желудочным соком, а также редуцируется до железистой и хелатной форм.
Вещества, которые формируют низкомолекулярное хелатное железо (такие как аскорбиновая кислота, сахар и аминокислоты), способствуют всасыванию железа.
Нормальная желудочная секреция содержит фактор стабилизации и вероятно эндогенный комплекс, который помогает замедлить осаждение поступающего с пищей железа в щелочном pH тонкой кишки.
Двухвалентная форма железа более растворима, чем трехвалентная его форма. Таким образом, двухвалентное железо легче пересекает слизистый слой с тем, чтобы достигнуть щеточной каймы тонкой кишки. Там оно окисляется до трехвалентного железа прежде, чем поступит в энтероцит.
В мембране эпителиальной клетки железо связывается с рецепторным белком, который перемещает его в клетку. Апотрансферрин цитозоля кишечных эпителиоцитов может ускорять абсорбцию железа. Скорость увеличивается при дефиците железа и, вероятно, это играет регулирующую роль, облегчая всасывание железа, когда потребность в нем увеличивается.
Большая часть железа, которое абсорбируется из просвета кишки, быстро проникает через эпителиоциты в форме небольших молекул. Железо, поступившее в плазму, окисляется церулоплазмином, который функционирует как ферроксидаза, и затем захватывается трансферрином . Этим путем обычно проходит 20–30 мг железа в сутки.
Часть цитозольного железа, которая превышает быструю транспортную вместимость, объединяется с апоферритином, формируя ферритин . Некоторое количество железа из ферритина позже может быть пущено в циркуляцию, но большее количество остается в клетках слизистой оболочки, пока они не слущиваются в просвет кишечника.
Прямое поступление железа в лимфатические сосуды незначительно. Ферритин синтезируется многими видами клеток, но преимущественно клетками печени и селезенки, являющимися основными депо железа в организме.
Скорость синтеза ферритина регулируется внутриклеточным содержанием железа, а часть образованного ферритина путем активной секреции или обратного эндоцитоза попадает в циркуляцию, причем количество циркулирующего в крови ферритина соответствует запасам железа.
Таким образом транспорт и депонирование железа осуществляются трансферрином , трансферриновым рецептором и ферритином.
К внеклеточным соединениям железа относят также лактоферрин, близкий по структуре к трансферрину, и гемсвязывающий белок — гемопексин.
Основным регулятором баланса железа является уровень абсорбции железа в ЖКТ. При дефиците железа в организме процесс абсорбции усиливается, а при избытке снижается. Всасывание железа происходит в тонком кишечнике и особенно интенсивно в энтероцитах двенадцатиперстной кишки.
Процесс всасывания железа начинается с миграции полипотентных клеток-предшественников, находящихся внутри кишечных крипт, на ворсинки. На заключительном этапе клетки-предшественники превращаются в зрелые эритроциты, способные к транспорту железа.
Метаболизм железа в организме здорового человека.
В ЖКТ абсорбируется всего 1 мг/сут железа. Поэтому основная потребность в железе удовлетворяется за счет его реутилизации из распадающихся эритроцитов, поддерживая постоянство баланса железа в организме, причем процессы реутилизации протекают достаточно интенсивно.
После абсорбции из ЖКТ железо транспортируется в плазму в основном в форме железа связанного с трансферрином . В дальнейшем комплекс железо-трансферрин взаимодействует с рецептором 1 трансферрина (RTf1), присутствующим в различных органах, в частности печени и эритропоетических клетках.
Период полужизни комплекса железо-трансферрин не превышает 60-90 мин. При усиленном эритропоэзе период полужизни комплекса сокращается до 10-15 мин.
В нормальных условиях большая часть железа (поступающего из кишечника (5%) и из рециклажа старых эритроцитов системы мононуклеарных макрофагов (95%)), транспортируемого троансферрином, переводится в костный мозг, где оно участвует в синтезе гемоглобина.
В костном мозге комплекс железо-трансферрин проникает в цитоплазму предшественников эритроцитов, в которых железо высвобождается из комплекса и встраивается в порфириновое кольцо гема. Гем включается в гемоглобин и в составе нового эритроцита железо покидает костный мозг.
Процесс транспортировки железа трансферрином в костный мозг осуществляется 10-20 раз в сутки. Ежедневно в организме взрослого человека обновляется 0,8% циркулирующих эритроцитов. В каждом 1 мл крови содержится 1 мг элементарного железа. Не утилизированное предшественниками эритроцитов железо запасается в селезенке, печени и костном мозге в виде ферритина.
При избытке пищевого или медикаментозного железа, несмотря на уменьшение его всасывания в процентном отношении, развивается перегрузка железом, последствия которой клинически манифестируют при гемолитических состояниях, частых гемотрансфузиях и у больных с гемохроматозом.
Источник: https://www.smed.ru/guides/43607